アルツハイマー病の発症や脳萎縮の原因となるタウ蛋白の蓄積を病初期段階から検出することは、現在開発中の抗タウ薬による早期治療を目指す上で重要です。私たちの研究グループは、アルツハイマー病患者のタウ蛋白の高感度、高精度検出が期待される新規PETトレーサーの候補化合物として、[18F]SNFT-1の開発に成功しました。従来型のタウPETトレーサーと比較して、[18F]SNFT-1は初期のタウ蛋白病変をより優れたコントラストで描出し、PETトレーサーに求められる薬物動態性能も満たしていました。今後、治療が必要なアルツハイマー病患者を早期発見するためのPET診断薬として、その臨床応用が期待されます。
SNFT-1はSendai Neuro Fibrillary-tangle Tracerの頭文字から命名された新規化合物です。これまでに開発されてきたアミロイドPETトレーサーやタウPETトレーサーと同様、18Fで標識可能な薬剤です。[18F]SNFT-1はアルツハイマー病患者の脳内で蓄積するタウ蛋白凝集物のみに結合し、オフターゲット結合の標的として過去に問題となったモノアミン酸化酵素B(MAO-B)には結合しません。またアミロイドβ線維などタウ蛋白以外の凝集物にも結合せず、アルツハイマー病のタウ病変に対する選択性が高いことが確認されています。
[18F]SNFT-1の病変検出感度について詳しく調べるため、認知症症状がないにもかかわらず、初期のアルツハイマー病の病理所見を示した高齢者の死後の脳病理組織標本を用いて評価を行いました。その結果、タウ病理の重症度としてはごく軽度に相当するブラークステージⅡの脳標本でも、[18F]SNFT-1はタウ病変を明瞭に描出しました(図1の赤矢頭で示した部分)。
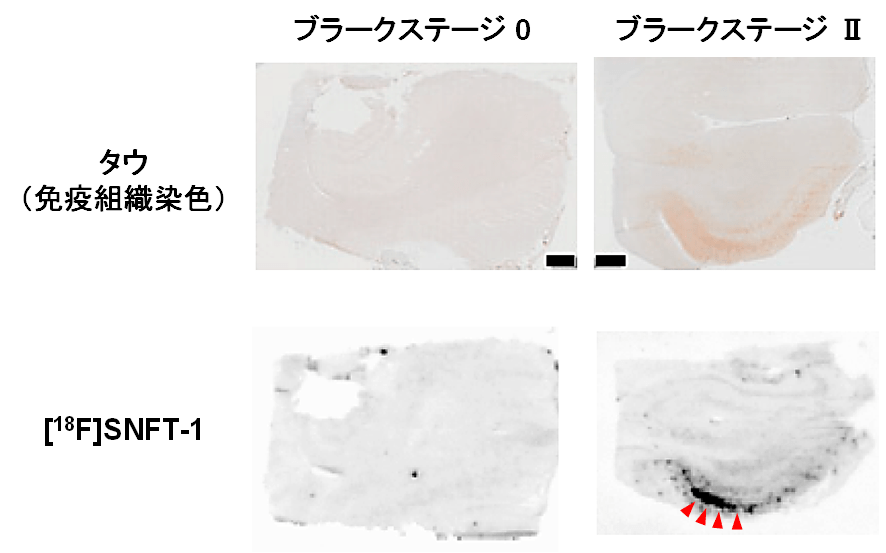
図1. 初期のタウ病変へ[18F]SNFT-1が結合したことを示すオートラジオグラフィー像
タウ病変がみられないブラークステージ0の脳標本(左)においては、[18F]SNFT-1の結合像は観察されません。これに対し、初期のタウ病変がみられるブラークステージⅡの脳標本(右)においては、タウの免疫組織染色と一致した[18F]SNFT-1の明瞭な結合像(赤矢頭)が観察されます。

図2. タウ病変部位での[18F]SNFT-1の信号強度を他のトレーサーと比較した結果
アルツハイマー病において病初期からタウ蓄積がみられやすい3つの場所(CA1、PHG、FuG)における[18F]SNFT-1の信号強度を既存の他のタウPETトレーサーと比較しました(図2)。その結果、ブラークステージⅡ(緑)およびステージⅥ(赤)のタウ病変を[18F]SNFT-1は最も高いコントラストで画像化することができました。よって従来型トレーサーよりも優れた感度でタウを検出できる可能性が示唆されました。さらに[18F]SNFT-1は、正常マウスに対して静脈内投与した際に、高い脳内取り込みと急速なウォッシュアウトを示したことから、PETトレーサーとして優れた性能を発揮するものと期待されます。
文献
Preclinical Characterization of the Tau PET Tracer [18F]SNFT-1: Comparison of Tau PET Tracers
Ryuichi Harada, Pradith Lerdsirisuk, Yuki Shimizu, Yuka Yokoyama, Yiqing Du, Kaede Kudo, Michinori Ezura, Yoichi Ishikawa, Ren Iwata, Miho Shidahara, Aiko Ishiki, Akio Kikuchi, Yuya Hatano, Tomohiko Ishihara, Osamu Onodera, Yasushi Iwasaki, Mari Yoshida, Yasuyuki Taki, Hiroyuki Arai, Yukitsuka Kudo, Kazuhiko Yanai, Shozo Furumoto and Nobuyuki Okamura
Journal of Nuclear Medicine (2023)
DOI:10.2967/jnumed.123.265593
URL: https://jnm.snmjournals.org/content/early/2023/06/15/jnumed.123.265593
